右美托咪定对行三叉神经微血管减压患者血清炎症因子及凝血功能的影响
王荣国1 丁文平1 刘 倩1 满园园2▲
1.江苏省徐州市中心医院麻醉科,江苏徐州 221009;2.江苏省徐州市中心医院呼吸科,江苏徐州 221009
[摘要] 目的 探究右美托咪定(DEX)对行三叉神经微血管减压患者围手术期血清炎症因子及凝血功能的影响。方法 选取2017 年1 月至2020 年10 月于徐州市中心医院收治的60 例行三叉神经微血管减压患者为研究对象,采用随机数字表法分为 DEX 组(30 例)和对照组(30 例)。 DEX 组给予 DEX 负荷剂量 1 μg/kg,维持剂量0.5 μg/(kg·h),对照组于同时间给予等量生理盐水。 比较两组手术时间,麻醉时间,观察预给药前(T0)、插管后(T1)、手术前 10 min(T2)、术后 1 h(T3)的心率(HR)、平均动脉压(MAP)的变化及肿瘤坏死因子-α(TNF-α)、白介素-6(IL-6)水平和凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)。 结果 两组的手术时间和麻醉时间比较,差异无统计学意义(P>0.05)。 两组 T0 时的 MAP、HR、TNF-α、IL-6 水平比较,差异无统计学意义(P>0.05);DEX 组T1、T2、T3 时间点 MAP、HR、TNF-α、IL-6 水平低于对照组,差异有统计学意义(P<0.05)。 两组 T0、T1、T2、T3 时 PT、APTT 水平比较,差异无统计学意义(P>0.05)。 结论 DEX 在三叉神经微血管减压术中麻醉效果显著,可有效减轻机体应激反应。 然而,没有明显证据表明右美托咪定的抗凝作用与抗炎作用之间存在联系,可能仅与其对患者的血流动力学改善有关。
[关键词]右美托咪定;显微血管减压术;炎症因子;凝血功能
显微血管减压术(microvascular decompression,MVD) 是治疗原发性三叉神经痛 (primary trigeminal neuralgia,PTN)的有效方法,即刻及长期疼痛缓解率较好[1]。PTN 作为神经病理性疼痛的一种,长期继续疼痛状态会导致患者外周血清炎症因子的过度表达[2-3]。而围手术期的应激反应也会引起患者机体炎症反应,并且在体内凝血与炎症也存在广泛关联[4]。 大量炎症因子的过度表达会对机体凝血功能产生一定影响,血液呈高凝状态,进而增加了术后深静脉血栓等并发症的发生风险,影响患者预后。 右美托咪定(Dexmedetomidine,DEX)是一种选择性肾上腺素能激动剂,对呼吸功能影响较小,具有抗焦虑、抗交感神经和镇痛镇静特性[5]。目前有研究表明DEX 对于神经病理性疼痛或手术应激所引起的机体炎症反应存有抑制作用,从而达到器官保护的作用[6-7]。 本研究选取60 例行三叉神经微血管减压术的患者为研究对象, 探究DEX 对患者围手术期血清炎症因子及凝血功能的影响。
1 资料与方法
1.1 一般资料
选取2017 年1 月至2020 年10 月于徐州市中心医院收治的60 例行三叉神经微血管减压患者为研究对象,采用随机数字表法分为DEX 组(30 例)和对照组(30 例)。 纳入标准:①择期行三叉神经微血管减压的患者;②ASA 分级Ⅰ~Ⅱ级;③年龄 40~65 岁。 排除标准:①术前血常规、凝血功能异常者;②近期服用抗凝、激素类或阿片类药物者;③放、化疗后的患者;④合并高血压或精神异常者; ⑤术中需要输血者;⑥目前应用肾上腺素能受体激动剂者; ⑦以往有药物过敏史者;⑧术前有心动过缓、房室传导阻滞、不稳定性心绞痛、急性心肌梗死、严重心瓣膜病及心衰者。 两组患者的性别、年龄及体重指数(body mass in dex,BMI)等一般资料比较,差异无统计学意义(P>0.05)(表1)。本研究得到徐州市中心医院医学伦理委员为批准,所有患者均同意参与本研究并签署知情同意书。
表1 两组患者的一般资料(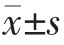 )
)
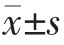 )
).jpg)
1.2 方法
1.2.1 麻醉方法 两组患者均采用相同方案行静脉麻醉,麻醉诱导采用静脉注射咪唑安定(江苏恩华药业,产品批号:MZ201703)0.05~0.1 μg/kg,芬太尼(宜昌人福药业,产品批号:01D03011)5 μg/kg,苯磺顺阿曲库铵(江苏新晨药业,产品批号200629AK)0.2 mg/kg,丙泊酚(江苏恩华,产品批号:16FD7326)1 mg/kg;持续泵入丙泊酚 6~8 μg/(kg·h),瑞芬太尼(宜昌人福药业,产品批号:20170120)0.1~0.2 μg/(kg·min), 每 45 分钟给予苯磺顺阿曲库铵5 mg。术中维持脉搏血氧饱和度(pulse oxygen saturation,SPO2)在 98%以上,呼气末二氧化碳分压(partial pressure of carbon dioxide in end expirationgas,PetCO2)在 35~45mmHg(1mmHg=0.133kPa),吸气氧浓度(fraction of inspiration O2,FiO2)0.8~1.0,根据血流动力学指标调整药物输注速度。术毕入麻醉复苏室(postanesthesia care unit,PACU)复苏。术后以舒芬太尼(宜昌人福药业,产品批号:01A07021)2 μg/kg+托烷司琼(西南药业,产品批号201706)10 mg 静脉自控镇痛。
1.2.2 试验干预 患者麻醉诱导开始前10 min 开始给予DEX 或生理盐水干预,其中DEX 组以DEX(江苏恒瑞医药股份有限公司,产品批号190903BP)1 μg/kg的负荷剂量 10 min 内静脉输注,后以 0.5 μg/(kg·h)的剂量维持至患者苏醒拔管。对照组静脉泵入等容量的生理盐水。 盲法控制:所有药物配制由另一名工作人员根据试验方案完成,患者、麻醉医师以及数据记录者对于所用药物及剂量不知情。
1.3 观察指标
入室后常规监测血压(arterial blood pressure,ABP)、心率(heart rate,HR)、心电图(electrocardiogram,ECG)、SPO2、平均动脉压(mean arterial pressure,MAP)、PetCO2。并行血气分析以及中心静脉压监测。 分别记录三组患者在围手术期各个时间点:DEX 预先给药前(T0)、插管后 10 min(T1)、手术结束前 10 min(T2)以及术后 1 h(T3)的 HR 和 MAP,并记录麻醉时间、手术时间。
标本采集及测定: 两组患者分别于麻醉诱导T0、T1、T2 以及T3 时,各抽取外周静脉血3 ml 两份并编号,其中一份 4°C, 离心 (离心半径 8 cm,4000 r/min)15 min 后取上清,置于-80°C 超低温冰箱中保存待测,另一份做常规凝血功能检测。 采用ELISA 法测定人血清中肿瘤坏死因子-α(tumor necrosis factor alpha,TNF-α)、白介素-6(interleukin-6,IL-6)的浓度水平。试剂盒购自上海恒远生物科技有限公司,上述操作均按照试剂盒说明书进行。 凝血指标检测方法:检查仪器为CA6000 凝血分析仪,采用凝固法测定凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partial thromboplastin time,APTT),分别记录各时间点PT、APTT 结果。
1.4 统计学方法
采用SPSS 24.0 统计学软件进行数据分析, 计量资料用均数±标准差(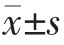 )表示,两组间比较采用t检验,重复测量资料采用重复测量方差分析;计数资料用率表示,组间比较采用χ2 检验,以P<0.05 为差异有统计学意义。
)表示,两组间比较采用t检验,重复测量资料采用重复测量方差分析;计数资料用率表示,组间比较采用χ2 检验,以P<0.05 为差异有统计学意义。
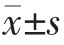 )表示,两组间比较采用t检验,重复测量资料采用重复测量方差分析;计数资料用率表示,组间比较采用χ2 检验,以P<0.05 为差异有统计学意义。
)表示,两组间比较采用t检验,重复测量资料采用重复测量方差分析;计数资料用率表示,组间比较采用χ2 检验,以P<0.05 为差异有统计学意义。2 结果
2.1 两组麻醉时间及手术时间的比较
两组患者的麻醉时间、手术时间比较,差异无统计学意义(P>0.05)(表 2)。
表2 两组麻醉时间及手术时间的比较(min,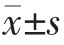 )
)
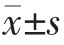 )
).jpg)
2.2 两组患者不同时间点MAP 及HR 的比较
整体分析发现:两组时间、组间、交互作用比较,差异有统计学意义(P<0.05)。 进一步两两比较,组内比较:两组 T1、T2、T3 时间点的 MAP 高于 T0,差异有统计学意义(P<0.05);对照组 T1、T2、T3 时间点的 HR 高于于 T0,差异有统计学意义(P<0.05);DEX 组 T1、T2、T3 时间点的 HR 低于 T0,差异有统计学意义(P<0.05)。组间比较:DEX 组 T1、T2、T3 时间点 MAP、HR 水平低于对照组,差异有统计学意义(P<0.05)(表 3)。
表3 两组患者不同时间点MAP 及HR 的比较(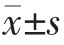 )
)
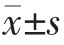 )
).jpg)
与本组 T0 比较,aP<0.05;与对照组同期比较,bP<0.05;1 mmHg=0.133 kPa
2.3 两组患者不同时间点炎症因子水平与凝血功能的比较
炎症因子表达水平整体分析发现: 两组时间、组间、交互作用比较,差异有统计学意义(P<0.05)。 进一步两两比较,组内比较:两组 T1、T2、T3 时间点 TNF-α、IL-6 水平高于 T0 时,差异有统计学意义(P<0.05)。 两组 T0 时 TNF-α、IL-6 水平比较, 差异无统计学意义(P>0.05);DEX 组 T1、T2、T3 时 TNF-α、IL-6 水平低于对照组,差异有统计学意义(P<0.05)。
凝血功能整体分析发现:两组时间、组间、交互作用比较,差异无统计学意义(P>0.05)。 两组 T0、T1、T2、T3 时 PT、APTT 水平比较,差异无统计学意义(P>0.05)(表 4)。
表4 两组患者不同时间点炎症因子水平与凝血功能的比较(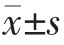 )
)
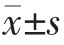 )
).jpg)
与本组T0 比较,aP<0.05;与对照组同期比较,bP<0.05
3 讨论
PTN 是中老年人常见的脑神经异常兴奋的疾病,可归因于第五脑神经根血管环的压迫,其病理学表现为脑神经根轴突确实或脱髓鞘,并由MVD 手术证实[8]。MVD 手术已经成为近几年治疗PTN 的重要手段,手术过程中应激反应的抑制对手术治疗效果有着重要的影响而选择合适的麻醉方法对提高MVD 手术成功率减少术后并发症尤为重要。
DEX 作为一种新型的高选择性α2-肾上腺素能受体拮抗剂,具有良好的镇静、镇痛以及交感神经抑制作用。 DEX 可减少心脏和周围脉管系统的交感神经或增强副交感神经的张力以改变血流动力学,对于手术患者在改善血流动力学稳定性, 降低应激反应,降低炎症水平,具有重要的临床意义[9-10]。 本研究结果显示, 以 1 μg/kg 的 DEX 负荷剂量,0.5 μg/(kg·h)的维持剂量给药, 患者整个手术过程中的HR 和MAP水平都低于术前以及对照组(P<0.05),提示其有利于血流动力学稳定, 考虑归因于DEX 可以抑制交感神经,减少PTN 患者术中的高血压反应,并通过激活运动神经元中的α2 受体来调节升高的血压。
有研究表明三叉神经痛可诱导机体多种炎症因子(TNF-α、IL-6、IL-8、IL-1β)的升高,而 IL-6 的浓度与PTN 严重程度呈正相关并可能在这些脑神经产生异位冲动的信号通路中起重要作用[11]。 手术麻醉及疼痛等应激反应同样能够影响机体内环境稳定,继发程度不一的炎症反应, 严重的炎症可以促发凝血反应,导致血栓栓塞时间的发生[12],反之,凝血反应也能够加重机体的炎症反应[13]。 有研究显示,手术患者应用DEX 可以有效的降低机体的应激反应, 减少由此导致的炎症反应[14-15];而且DEX 对于改善围手术期机体凝血功能中也有一定的作用, 其认为DEX 对术后凝血激活的抑制作用归因于DEX 的抗交感活性的特性[16-17]。 DEX 也可以直接刺激血小板表面的α2-肾上腺素受体并激活血小板[18];并且DEX 也抑制交感神经平并减少儿茶酚胺的释放,从而间接抑制血小板功能[19]。 因此此前本研究认为DEX 也有可能通过抑制炎症反应从而改善术中凝血功能。 本项研究显示,DEX 组的TNF-α、IL-6 的表达水平相比较对照组有明显的降低,与前期其他研究结果相一致[20];而在对凝血功能的检测中DEX 组的PT、APTT 与对照组比较,差异无统计学意义(P>0.05),提示在三叉神经显微血管减压手术中应用DEX 虽然其对手术患者的炎症反应有抑制作用,但其通过抑制炎症反应改善术中及术后凝血功能的假想缺乏证据支持。
综上所述, 在显微血管减压手术中应用DEX 可有效的保持三叉神经痛患者的血流动力学的稳定,而且降低机体的应激反应有利于机体内环境的稳定。 尽管DEX 对于围手术期患者的炎症反应具有明显的抑制作用, 但是其对患者术中及术后的凝血功能的影响与其抗炎作用并无表现出有明显的关联,考虑本研究中DEX 应用时间短等诸多因素,DEX 对三叉神经痛手术患者围手术期的凝血功能的影响有待进一步研究。
[参考文献]
[1]Zheng JH,Sun K,Zhan HT,et al.A Study on the Recurrence Rate of Trigeminal Neuralgia after MVD and the Related Factors[J].J Neurol Surg B Skull Base,2020,81(5):572-578.
[2]Sommer C,Leinders M,Uceyler N.Leinders and N.Uceyler.Inflammation in the pathophysiology of neuropathic pain[J].Pain,2018,159(3):595-602.
[3]Gerwin R.Chronic Facial Pain:Trigeminal Neuralgia,Persistent Idiopathic Facial Pain,and Myofascial Pain Syndrome-An Evidence-Based Narrative Review and Etiological Hypothesis[J].Int J Environ Res Public Health,2020,17(19):543-547.
[4]Paparella D,Rotunno C,Guida P,et al.Minimally invasive heart valve surgery:influence on coagulation and inflammatory response [J].Interact Cardiovasc Thorac Surg,2017,25(2):225-232.
[5]Weerink M,Struys M,Hannivoort L,et al.Clinical Pharmacokinetics and Pharmacodynamics of Dexmedetomidine[J].Clin Pharmacokinet,2017,56(8):893-913.
[6]Guo YB,Xu JD,Ji XX,et al.Protective effect of dexmedetomidine against perioperative inflammation and on pulmonary function in patients undergoing radical resection of lung cancer[J].Nan Fang Yi Ke Da Xue Xue Bao,2017,37(12):1673-1677.
[7]Keating GM.Dexmedetomidine:A Review of Its Use for Sedation in the Intensive Care Setting[J].Drugs,2015,75(10):1119-1130.
[8]Zhong J,Zhu J,Sun H,et al.Microvascular decompression surgery:surgical principles and technical nuances based on 4000 cases[J].Neurol Res,2014,36(10):882-893.
[9]Wang L,Zhang A,Liu W,et al.Effects of dexmedetomidine on perioperative stress response,inflammation and immune function in patients with different degrees of liver cirrhosis[J].Exp Ther Med,2018,16(5):3869-3874.
[10]Devcic A,Schmeling WT,Kampine JP,et al.Oral dexmedetomidine preserves baroreceptor function and decreases anesthetic requirements of halothane-anesthetized dogs[J].Anesthesiology,1994,81(2):419-430.
[11]Liu MX,Zhong J,Xia L,et al.A correlative analysis between inflammatory cytokines and trigeminal neuralgia or hemifacial spasm[J].Neurol Res,2019,41(4):335-340.
[12]Esmon C.The interactions between inflammation and coagulation[J].Br J Haematol,2005,131(4):417-430.
[13]Kawamoto S,Hirakata H,Sugita N.Bidirectional relation between inflammation and coagulation[J].Circulation,2004,109(22):2698-704.
[14]Guo YB,Xu JD,Ji XX,et al.Protective effect of dexmedetomidine against perioperative inflammation and on pulmonary function in patients undergoing radical resection of lung cancer[J].Nan Fang Yi Ke Da Xue Xue Bao,2017,37(12):1673-1677.
[15]Kong L,Lu XH.Effect of dexmedetomidine on perioperative inflammatory response and cellular immune in patients undergoing radical operation of thoracoscopic lung cancer[J].Zhonghua Yi Xue Za Zhi,2018,98(36):2929-2932.
[16]Zhao L,Li Y.Application of de xmedetomidine combined with sufentanil in colon cancer resection and its effect on immune and coagulation function of patients[J].Oncol Lett,2020,20(2):1288-1294.
[17]Chen Z,Shao DH,Mao ZM,et al.Effect of dexmedetomidine on blood coagulation in patients undergoing radical gastrectomy under general anesthesia:A prospective,randomized controlled clinical trial[J].Medicine (Baltimore),2018,97(27):111-119.
[18]Kawamoto S,Hirakata H,Sugita N,et al.Bidirectional effects of dexmedetomidine on human platelet functions in vitro[J].Eur J Pharmacol,2015,766:122-128.
[19]Martins C,Tardelli MA,Amaral JL.Tardelli and J.L.Amaral.Effects of dexmedetomidine on blood coagulation evaluated by thromboelastography[J].Rev Bras Anestesiol,2003,53(6):705-719.
[20]Wang K,Wu M,Xu J,et al.Effects of dexmedetomidine on perioperative stress,inflammation,and immune function:systematic review and meta-analysis[J].Br J Anaesth,2019,123(6):777-794.
Effect of Dexmedetomidine on inflammatory cytokines and coagulation function of the patients undergoing microvascular decompression surgery
WANG Rong-guo1 DING Wen-ping1 LIU Qian1 MAN Yuan-yuan2▲
1. Department of Anesthesiology, Xuzhou Central Hospital, Jiangsu Province, Xuzhou 221009, China; 2. Department of Respiratory, Xuzhou Central Hospital, Jiangsu Province, Xuzhou 221009, China
1. Department of Anesthesiology, Xuzhou Central Hospital, Jiangsu Province, Xuzhou 221009, China; 2. Department of Respiratory, Xuzhou Central Hospital, Jiangsu Province, Xuzhou 221009, China
[Abstract] Objective To investigate the effects of Dexmedetomidine (DEX) on serum inflammatory factors and coagulation function in perioperative patients undergoing trigeminal nerve microvascular decompression. Methods A total of 60 patients with trigeminal nerve microvascular decompression admitted to Xuzhou Central Hospital from January 2017 to October 2020 were selected as the study subjects,and were divided into DEX group(30 cases)and control group(30 cases)by random number table method. DEX group was given DEX load dose of 1 μg/kg, maintenance dose of 0.5 μg/ (kg·h),and control group was given normal saline at the same time. Operation time and anesthesia time were compared between the two groups, and changes of heart rate (HR) and mean arterial pressure (MAP), tumor necrosis factor-α (TNF-α),interleukin-6 (IL-6) levels and prothrombin time (PT), activated partial thrombin time (APTT) were observed before drug administration (T0), after intubation (T1), 10 min before surgery (T2), and 1 h after surgery (T3). Results There was no significant difference in operation time and anesthesia time between the two groups (P>0.05). There were no significant differences in MAP, HR, TNF-α and IL-6 levels between the two groups at T0 (P>0.05). MAP, HR, TNF-α and IL-6 levels at T1, T2 and T3 in DEX group were lower than those in control group, the differences were statistically significant (P<0.05). There were no significant differences in PT and APTT levels between the two groups at T0, T1, T2 and T3(P>0.05). Conclusion DEX has a significant anesthetic effect in trigeminal microvascular decompression, and can effectively reduced the stress response of the body. However, there is no obvious evidence to link the coagulation function enhancement of DEX with its inhibitory effects on inflammatory responses, which might be just associated with its attenuation effects on hemodynamics of patients.
[Key words] Dexmedetomidine; Microvascular decompression surgery; Coagulation function; Inflammatory response
[中图分类号] R614
[文献标识码] A
[文章编号] 1674-4721(2021)12(a)-0139-05
[作者简介]王荣国(1982-),男,硕士,副主任医师,研究方向:围手术期认知功功能障碍机制,主要从事临床麻醉工作。
▲通讯作者
(收稿日期:2021-01-27)