骨疏宁口服液的安全剂量及长期毒性研究
吴勇梅1 梁志敏1 韦玉燕1 覃 良2▲
1.广西壮族自治区玉林市中西医结合骨科医院药剂科,广西玉林 537000;2.广西壮族自治区中医药研究院药理室,广西南宁 530022
[摘要]目的 观察长期重复给予骨疏宁口服液对大鼠所产生的毒性反应及安全剂量。方法 选取80 只SD 大鼠作为研究对象,按照随机分组的方法分为低、中、高剂量组和对照组,每组20 只。低、中、高剂量组分别给予骨疏宁口服液5.38、10.76、21.50 g 药材/(kg·d),对照组给予等体积蒸馏水,分别连续灌胃12 周。给药期间每日观察动物一般表现及毒性反应情况,停药后恢复2 周,进行常规毒理学观察和血液学、血液生化学指标检测并进行比较。结果 低、中、高剂量组的体重增长正常,与对照组比较差异无统计学意义(P>0.05);低、中、高剂量组的血液学检查及血液生化学检查与对照组比较,差异无统计学意义(P>0.05)。主要脏器的病理组织学检查中,各指标未见因药物毒性引起的明显病理改变。结论 骨疏宁口服液对大鼠灌胃给药的安全剂量为21.50 g 药材/(kg·d),相当于临床成人每日剂量的120 倍,长期重复给药未见毒性反应。
[关键词]骨疏宁口服液;长期毒性;安全剂量
骨疏宁口服液来源于全国名老中医赖祥林的经验方,由淫羊藿、骨碎补、制何首乌、丹参、续断、仙茅、蜈蚣等中药组成,按照最佳工艺制得[1],用于治疗原发性骨质疏松症及骨质疏松症引起的骨折、骨痛等症[2-5]。处方中仙茅和蜈蚣均为现行版《中国药典》标识“有毒”的药材[6],多疗程连续服用该制剂是否安全值得探讨。为了给骨疏宁口服液临床用药安全提供可靠的实验数据, 本研究根据中药新药研究指南、中药、天然药物长期毒性研究技术指导原则等法规[7-8],通过大鼠长期毒性试验,观察骨疏宁口服液对大鼠有关生理生化功能的影响, 进行安全性评价,探讨安全剂量。
1 材料与方法
1.1 实验动物
Wistar 大鼠,体重130~160 g,雌雄各半,由广西医科大学实验动物中心提供,生产许可证号为SCXK桂2014-0002。
1.2 实验药物
骨疏宁口服液由玉林市中西医结合骨科医院提供(批号:20180223)。每毫升含药材0.538 g,成人用量每日2 次,每次10 mL。将药液浓缩至每毫升含药材1.076 g 供试验用。
1.3 实验仪器
BS-600 全自动生化分析仪购自深圳迈瑞公司;BC-2800 Vet 全自动血细胞分析仪购自深圳迈瑞公司;Leica DM 2500 显微成像分析系统购自Leica 仪器(德国)有限公司。
1.4 实验方法
选取80 只雌雄各半、体重均在130~160 g 之间的健康SD 大鼠作为研究对象,按照随机分组的方法分为低、中、高剂量组和对照组,每组20 只。低、中、高剂量组分别给予骨疏宁口服液5.38、10.76、21.50 g 药材/(kg·d),分别相当于本品临床日剂量(10.76 g 药材/60 kg 体重)的30、60、120 倍,对照组给予等体积蒸馏水。模拟骨疏宁口服液临床给药途径,灌胃给药,给药量每天20 mL/kg 体重,连续灌胃12 周。给药后每周根据体重调节给药量。试验期间每天观察动物的一般表现以及毒性反应情况,如外观体征、行为活动、尿、粪便性状、饮食等, 每周称量大鼠体重及进食量各1次。末次给药后第2 天,每组取12 只大鼠处死,测定血液学和血液生化指标,计算各个大鼠主要脏器每100 g 体重相应脏器系数,并对主要脏器进行病理组织学检查。其余动物停药后观察2 周,同法检测以上指标。
1.5 观察指标
比较各组大鼠的一般表现、血液学指标、血液生化学指标以及进行病理组织学检查,具体如下。
1.5.1 一般表现 观察外观体征、体重、呼吸、腺体分泌、粪便、日摄食量、行为活动、给药局部反应。
1.5.2 血液学指标 包括血红蛋白(Hb)、平均红细胞血红蛋白(MCHC)、平均红细胞血红蛋白浓度(MCH)、红细胞计数(RBC)、红细胞压积(HCT)、平均红细胞容积(MCV)、网织红细胞计数(RC)、血小板计数(PLT)、白细胞计数(WBC)及其分类[粒细胞(GRA)、淋巴细胞(LYM)、单核细胞(MON)、凝血酶原时间(PT)]。
1.5.3 血液生化学指标 包括清蛋白(ALB)、血清总蛋白(TP)、谷丙转氨酶(ALT)、天门冬氨酸转氨酶(AST)、血清总胆红素(TBil)、尿素氮(BUN)、肌酐(Cr)、碱性磷酸酶(ALP)、总胆固醇(TC)、三酰甘油(TG)、葡萄糖(GLU)、肌酸磷酸激酶(CK)、钠离子浓度(Na+)、钾离子浓度(K+)、氯离子浓度(Cl-)。
1.5.4 病理组织学检查 主要包括心、肝、肾、肺、胃、脾、小肠、大肠、胰腺、甲状腺、胸腺、肾上腺、大脑、小脑、脑垂体、食管、气管、脊髓、主动脉、睾丸、附睾、前列腺、膀胱、卵巢、子宫、骨髓、坐骨神经的肉眼观察和组织学检查,并对心、肝、肾、肺、脾、胸腺、肾上腺、脑、卵巢、子宫称重,分别计算脏器系数(脏器重量/体重)。
1.6 统计学方法
采用SPSS 22.0 统计学软件进行数据处理,符合正态分布的计量资料用均数±标准差(.jpg) ±s)表示,多组间比较采用方差分析,不符合正态分布者转换为正态分布后行统计学分析,以P<0.05 为差异有统计学意义。
±s)表示,多组间比较采用方差分析,不符合正态分布者转换为正态分布后行统计学分析,以P<0.05 为差异有统计学意义。
2 结果
2.1 各组的一般表现分析
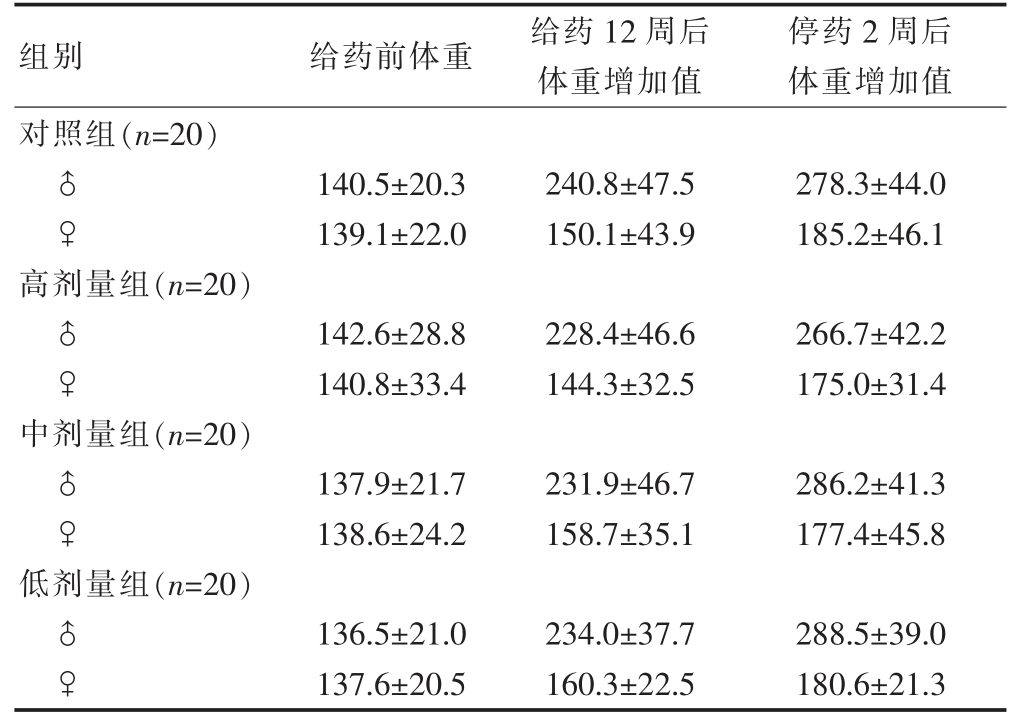
低、中、高剂量组及对照组动物的外观体征、呼吸、日摄食量、腺体分泌、粪便、给药局部反应、体重增长等均正常,未见明显毒性反应。低、中、高剂量组动物的体重增长与对照组比较,差异无统计学意义(P>0.05)(表1)。
表1 骨疏宁口服液给药3 个月大鼠体重增长情况(g,.jpg) ±s)
±s)
2.2 各组血液学检查指标的比较
低、中、高剂量组给药12 周和停药2 周的血液学检查指标与对照组比较,差异无统计学意义(P>0.05)(表2)。
2.3 各组血液生化学检查的比较
给药12 周,骨疏宁口服液高剂量组的ALT 值有波动,但与对照组比较差异无统计学意义(P>0.05)。其余各指标未见异常。停药2 周,低、中、高剂量组与对照组各指标检测值比较,差异无统计学意义(P>0.05)(表3)。
2.4 各组脏器系数检查的比较
给药12 周及停药2 周,低、中、高剂量组大鼠与正常对照组大鼠的脏器系数比较,差异无统计学意义(P>0.05)(表4)。
表2 各组骨疏宁口服液血液学测定值的比较(.jpg) ±s)
±s)
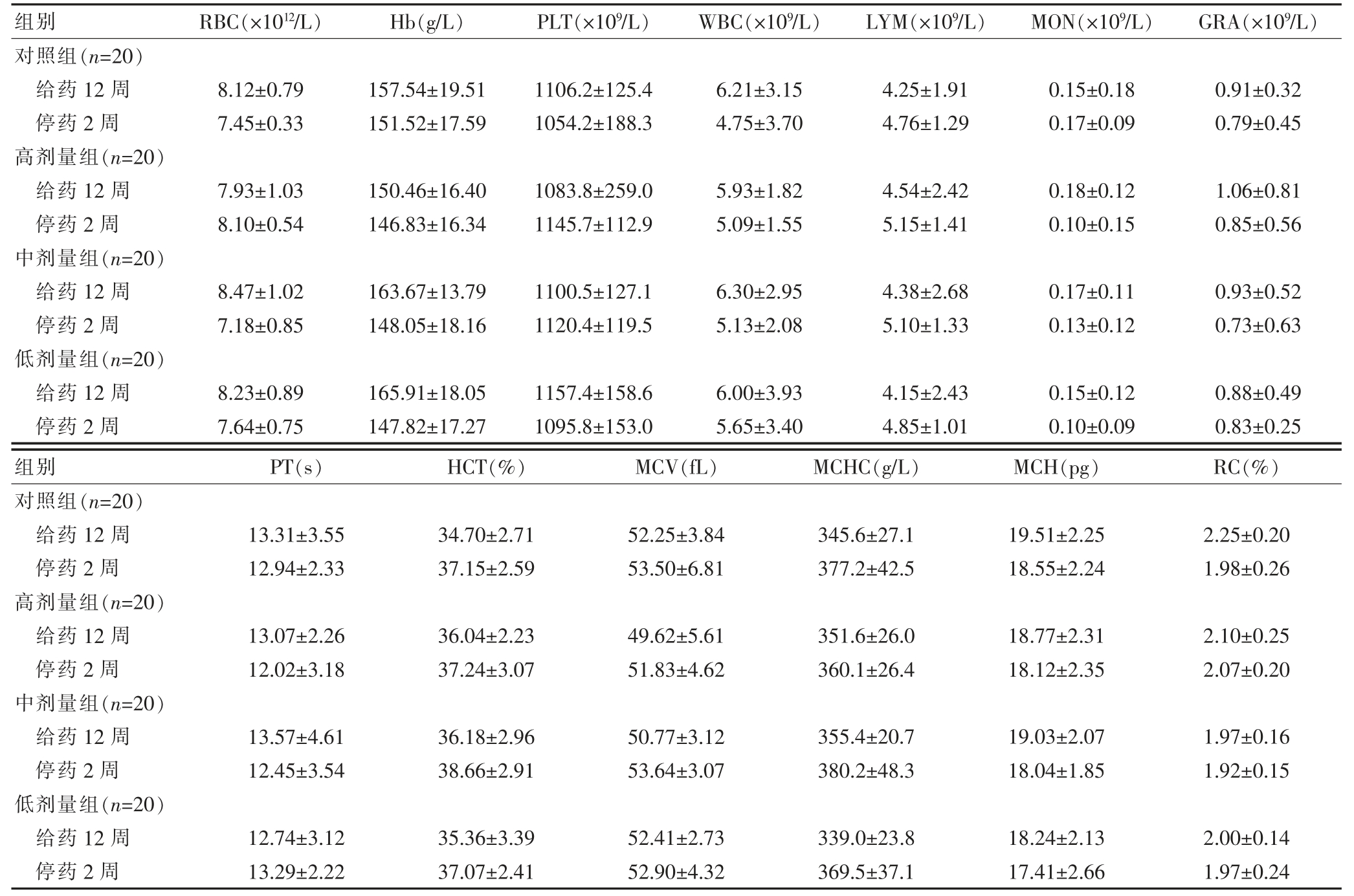
表3 各组骨疏宁口服液大鼠血液生化测定值的比较(.jpg) ±s)
±s)

表4 各组骨疏宁口服液大鼠主要脏器系数值的比较(g/100 g 体重,.jpg) ±s)
±s)

2.5 主要脏器的病理组织学检查
部分动物在停药24 h 和停药14 d 出现间质性肝炎、肝轻度脂肪变性、间质性肾炎,低、中、高剂量组及对照组均有部分动物出现,属于动物的常见病及多发病,可排除因药物引起,表明骨疏宁口服液在该剂量下对大鼠无因药物毒性引起的主要器官病理形态学改变(图1~5)。
.jpg)
图1 给药组心脏病理改变
心肌纤维呈分枝状排列, 核位于纤维中部, 胞浆细腻, 间质清晰(HE,400×)
.jpg)
图2 对照组心脏病理改变
心肌纤维呈分枝状排列, 核位于纤维中部, 胞浆细腻, 间质清晰(HE,400×)
3 讨论
.jpg)
图3 给药组肝脏病理改变
肝中央静脉位于小叶中心,四周肝细胞排列整剂,胞浆细腻,枯否氏细胞散在性分布(HE,400×)
.jpg)
图4 对照组肝脏病理改变
肝中央静脉位于小叶中心,四周肝细胞排列整剂,胞浆细腻,枯否氏细胞散在性分布(HE,400×)
.jpg)
图5 给药组肾脏病理改变
肾单位结构和上皮细胞形态正常, 管腔和间质未见其他物质沉积(HE,400×)
骨疏宁口服液处方中含有毒药材仙茅和蜈蚣,仙茅毒性的物质基础研究较少, 其毒性也可能是大剂量的活性成分引起。曾有仙茅不良反应和毒性反应的报道, 有学者认为临床中长期服用仙茅还是存在一定安全隐患[9-12]。蜈蚣药材具有致过敏、致炎、神经毒性、局部组织损伤及溶血、心肌损伤、致痛等物质基础,可出现致过敏、肝肾毒性、妊娠毒性、神经毒性等毒副作用[13-15]。骨疏宁口服液为医院制剂,对含有有毒药材的制剂进行长期毒性考察,是医疗机构制剂注册管理办法中制剂申报注册的研究内容,同时也为骨疏宁方在临床应用多年的安全性提供实验数据证明。
本实验通过骨疏宁口服液分别以5.38、10.76、21.50 g 药材/(kg·d)[分别相当于临床成年人每日剂量0.179 g 药材/(kg·d)的30、60、120 倍]给予大鼠灌胃给药12 周,停药2 周后检查,结果未见大鼠的外观体征、腺体分泌、呼吸、粪便、饲料日消耗量、给药局部反应等一般状况出现异常和明显毒性反应。低、中、高剂量组大鼠的体重增长、血液学及血液生化学检查与对照组比较差异均无统计学意义(P>0.05)。主要脏器的系数无明显变化,且病理组织学检查未见因药物毒性引起的明显病理改变。上述结果表明,经口对大鼠灌胃给予骨疏宁口服液21.50 g 药材/kg 体重(相当于临床成人每日剂量的120 倍)的剂量是安全的,该制剂长期重复给药未见毒性反应。
[参考文献]
[1]韦玉燕,吴勇梅,何科.骨疏宁口服液提取工艺的研究[J].中国民族民间医药,2018,27(11):33-36.
[2]吕琳,庞声航,曾翠琼,等.骨疏宁颗粒对维甲酸致大鼠骨质疏松的影响[J].广西中医学院学报,2008,11(1):3-5.
[3]庞声航,曾翠琼,吕琳,等.骨疏宁颗粒治疗去卵巢后骨质疏松大鼠的实验研究[J].广西中医药,2008,31(2):54-56.
[4]李永斌,李开静,赖祥林.骨疏宁治疗原发性骨质疏松症骨痛63 例[J].辽宁中医药大学学报,2007,9(6):115.
[5]陈涛,黎观保,贾世青,等.经皮椎体成形术联合骨疏宁片治疗胸腰椎椎体骨折的临床疗效分析[J].中国临床新医学,2016,9(3):201-204.
[6]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:102,357.
[7]中华人民共和国卫生部药政管理局.中药新药研究指南(药学、药理学、毒理学)[M].北京:中华人民共和国卫生部药政管理局,1994:205
[8]国家食品药品监督管理局.中药、天然药物长期毒性研究技术指导原则[EB/OL].(2005-03).http://www.360doc.com/document/17/0818/19/363181_680228586.shtml.
[9]王霖,张雪,孔令雷,等.仙茅等有小毒记载的祛风除湿中药毒性的历史认识与评价[J].中药药理与临床,2018,34(5):157-160.
[10]陈洪雷.仙茅提取物的毒性实验研究[D].曲阜:曲阜师范大学,2011.
[11]朱芳芳,杨明华,陈婉姬,等.不同配伍比例仙茅-淫羊藿药对的毒性与含量相关性[J].中国实验方剂学杂志,2015,21(5):175-177.
[12]钟捷,陈艳,周德生.仙茅等中药致药物中毒性周围神经病1 例[J].现代中西医结合杂志,2010,19(24):3107-3108.
[13]于金高,刘培,段金廒.药用蜈蚣生物活性物质与毒性物质研究进展[J].中国现代中药,2016,18(11):1521-1527.
[14]车景超.中药娱蚣药用历史沿革及其安全性探讨[J].中医临床研究,2013,5(12):118-119.
[15]田莎,田雪飞,黄晓蒂,等.蜈蚣药理作用、临床用量及毒性研究概况[J].湖南中医杂志,2018,34(5):212-214.
Study on safety dose and long-term toxicity of Gushuning Oral Liquid
WU Yong-mei1 LIANG Zhi-min1 WEI Yu-yan1 QIN Liang2▲
1. Department of Pharmacy, Hospital of Integrated Traditional Chinese and Western Medicine of Yulin City, Guangxi Zhuang Autonomous Region, Yulin 537000, China; 2. Department of Pharmacology, Guangxi Zhuang Autonomous Region Institute of Traditional Chinese Medicine, Guangxi Zhuang Autonomous Region, Nanning 530022, China
1. Department of Pharmacy, Hospital of Integrated Traditional Chinese and Western Medicine of Yulin City, Guangxi Zhuang Autonomous Region, Yulin 537000, China; 2. Department of Pharmacology, Guangxi Zhuang Autonomous Region Institute of Traditional Chinese Medicine, Guangxi Zhuang Autonomous Region, Nanning 530022, China
[Abstract] Objective To observe the toxicity and safe dose of Gushuning Oral Liquid in rats after long-term repeated administration. Methods A total of 80 SD rats were selected and randomly divided into the low, middle, high dose group and the control group, 20 rats in each group. The low, middle and high dose groups were given Gushuning Oral Liquid 5.38, 10.76, 21.50 g medicine/(kg·d), respectively, and the control group were given equal volume distilled water, which were were gavaged for 12 weeks. During the period of administration, the general performance and toxic reaction of animals were observed daily, and recovered for 2 weeks after discontinuation. Routine toxicological observation and hematological and biochemical indexes were detected and compared. Results The weight gain of the low,medium and high dose groups were normal, and there was no significant difference compared with the control group (P>0.05). There was no significant difference in hematological examination and blood biochemical examination between the low, medium and high dose groups and the control group (P>0.05). In the histopathological examination of main organs,there was no obvious pathological change caused by drug toxicity. Conclusion The safe dose of Gushuning Oral Liquid to rats by gavage is 21.50 g medicine/(kg·d), which is 120 times of the daily dose of clinical adults. There is no toxic reaction after long-term repeated administration.
[Key words] Gushuning Oral Liquid; Long-term toxicity; Safe dose
[中图分类号] R332
[文献标识码] A
[文章编号] 1674-4721(2021)1(c)-0008-05
[基金项目]广西壮族自治区卫生厅中医药医院制剂类课题项目(GZYZ-10-50)
[作者简介]吴勇梅(1971-),女,副主任药师,研究方向:医院制剂研究开发
▲通讯作者:覃良(1965-),男,副主任药师,研究方向:新药研究开发
(收稿日期:2020-05-20)