左乙拉西坦治疗小儿热性惊厥的临床效果
廖月娟
广东省人民医院珠海医院儿科,广东广州 519000
[摘要]目的 研究左乙拉西坦治疗小儿热性惊厥的临床效果。方法 选取2017年5月~2019年1月我院收治的96例热性惊厥患儿作为研究对象,依据随机数字表法将其分为对照组和观察组,每组各48 例。对照组患儿进行常规治疗,观察组患儿在对照组的基础上使用左乙拉西坦治疗。比较分析两组患儿的临床疗效及不良反应发生情况。记录两组患儿的症状缓解情况及治疗前后脑神经相关因子[神经元特异性烯醇化酶(NSE)、S-100β 蛋白(S-100β)、脑源性神经营养因子(BDNF)]水平。结果 观察组患儿的治疗总有效率(95.83%)高于对照组(83.33%),退热时间早于对照组,差异有统计学意义(P<0.05)。治疗后,观察组患儿的NSE、S-100β、BDNF 水平均低于对照组,差异有统计学意义(P<0.05)。两组患儿的发热次数及不良反应发生率比较,差异无统计学意义(P>0.05)。结论 左乙拉西坦治疗小儿热性惊厥,能够显著提升临床疗效,更快缓解患儿发热症状,大幅改善脑神经相关因子水平,同时保障了用药安全性,对患儿预后具有积极作用。
[关键词]小儿热性惊厥;左乙拉西坦;脑神经相关因子;癫痫
小儿热性惊厥是儿科及神经内科高发病症,属于小儿最常见惊厥之一。热性惊厥预后普遍良好,患儿6 岁后大脑基本发育完善,从而惊厥可有效缓解[1-2]。热性惊厥多发于6 个月~3 岁小儿群体,且年龄越小发生率越高。一般发生在上呼吸道等感染性疾病初期,体温升高是最显著的症状,多在体温高于38℃时出现惊厥[3-4]。目前,临床以安定止惊及常规退热等手段治疗小儿热性惊厥,但对于病情较严重患儿效果甚微,有研究认为抗癫痫药物左乙拉西坦对小儿热性惊厥具有一定疗效[5]。为明确其临床应用价值,给予患儿更加安全、有效的治疗方法,展开相关对比研究,现报道如下。
1 资料与方法
1.1 一般资料
选取2017年5月~2019年1月我院收治的96例热性惊厥患儿作为研究对象,依据随机数字表法将其分为对照组和观察组,每组各48 例。观察组中,男27例,女21 例;年龄9~63 个月,平均(29.30±10.52)个月;发病年龄6~28 个月,平均(11.29±3.62)个月;病程1~19个月,平均(9.43±3.12)个月;家族病史:有家族史19 例,无家族史29 例;热性惊厥发作性质:单纯性41例,复杂性7 例。对照组中,男25 例,女23 例;年龄10~61 个月,平均(30.27±11.44)个月;发病年龄6~27个月,平均(11.17±3.59)个月;病程1~22 个月,平均(9.56±3.07)个月;家族病史:有家族史18 例,无家族史30 例;热性惊厥发作性质:单纯性42 例,复杂性6例。两组患儿的性别、年龄、发病年龄、病程、家族史及热性惊厥发作性质等一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究在经过我院医学伦理委员会同意后开展。
1.2 纳入及排除标准
纳入标准:①患儿均符合《热性惊厥诊断治疗与管理专家共识2016》[6]中相关诊断标准,并经血生化、脑电图、头颅CT 等检查后确诊;②患儿均对本研究中所使用治疗药物无过敏史,且通过治疗前试敏实验;③所有患儿均未合并代谢性异常疾病;④患儿父母或其他法定监护人均在了解本研究详情后自愿签署知情同意书。
排除标准:①合并心、肝、肾、肺功能严重损伤患儿;②合并颅内感染或发育不良患儿;③中途退出或未定时复查、未完成随访资料统计患儿。
1.3 方法
对照组患儿进行常规治疗,方法如下。将患儿保持平侧卧位,以此防止呕吐物吸入导致窒息,体温不足38℃时使用温水擦拭进行物理降温,体温高于38℃时给予药物退热,根据病情实施解痉止挛措施并维持水电解质平衡,必要时给予营养支持。
观察组患儿在对照组的基础上使用左乙拉西坦片(浙江京新药业股份有限公司,生产批号:20170310、20180502)治疗,治疗第1~7 天用量为15 mg/kg,2 次/d;第8~12 天用量为10 mg/kg,2 次/d,第13~15 天为5 mg/kg,2 次/d。两组患儿均治疗15 d。
1.4 观察指标及评价标准
比较分析两组患儿的临床疗效及不良反应发生情况。记录两组患儿的症状缓解情况及治疗前后脑神经相关因子[神经元特异性烯醇化酶(NSE)、S-100β蛋白(S-100β)、脑源性神经营养因子(BDNF)]水平。
①临床疗效:疗效标准参照《热性惊厥诊断治疗与管理专家共识2017》[7]中相关内容,治疗后3 d 内,患儿体温恢复正常,且未复发惊厥为显效;治疗后患儿5 d 内体温恢复正常,且未复发惊厥为有效;治疗后患儿高热、惊厥等症状无改善或病情加重为无效。总有效=有效+显效。②症状缓解情况:统计两组退热时间并进行6 个月的随访,比较期间两组患儿的发热次数。③脑神经相关因子:于治疗前及治疗后清晨,患儿处空腹状态下抽取静脉血2 ml,以3500 r/min 进行离心分离,得到血清后使用酶联免疫吸附法测定血清NSE、S-100β、BDNF 水平变化情况。④不良反应发生情况:随访并统计两组患儿嗜睡、情绪易激、食欲减退、乏力发生情况。
1.5 统计学方法
采用SPSS 21.0 统计学软件进行数据分析,计量资料用均数±标准差(.jpg) ±s)表示,两组间比较采用t 检验;计数资料采用率表示,组间比较采用χ2 检验;等级资料采用秩和检验,以P<0.05 为差异有统计学意义。
±s)表示,两组间比较采用t 检验;计数资料采用率表示,组间比较采用χ2 检验;等级资料采用秩和检验,以P<0.05 为差异有统计学意义。
2 结果
2.1 两组患儿临床疗效的比较
观察组的临床效果优于对照组(P<0.05);观察组患儿的治疗总有效率(95.83%)高于对照组(83.33%),差异有统计学意义(P<0.05)(表1)。
表1 两组患儿临床疗效的比较[n(%)]
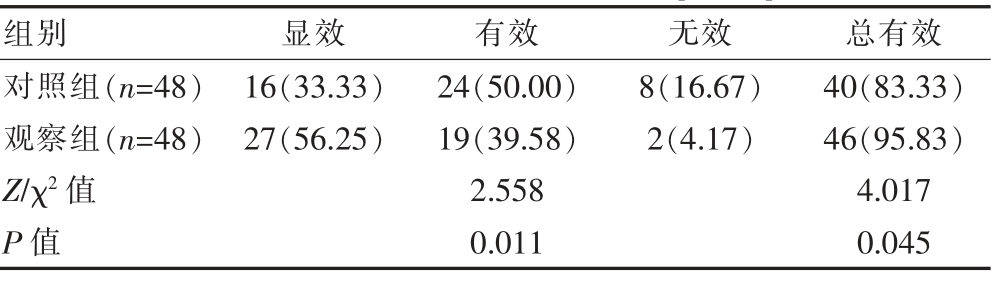
2.2 两组患儿症状缓解情况的比较
两组患儿的发热次数比较,差异无统计学意义(P>0.05);观察组患儿的退热时间早于对照组,差异有统计学意义(P<0.05)(表2)。
表2 两组患儿症状缓解情况的比较(.jpg) ±s)
±s)
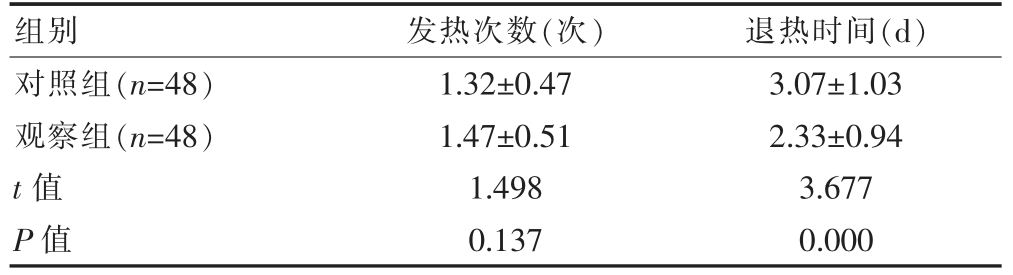
2.3 两组患儿治疗前后脑神经相关因子水平的比较
两组患儿治疗前的脑神经相关因子水平比较,差异无统计学意义(P>0.05);两组患儿治疗后的NSE、S-100β、BDNF 水平均低于治疗前,差异有统计学意义(P<0.05)。治疗后,观察组患儿的NSE、S-100β、BDNF 水平均低于对照组,差异有统计学意义(P<0.05)(表3)。
表3 两组患儿治疗前后脑神经相关因子水平的比较(.jpg) ±s)
±s)
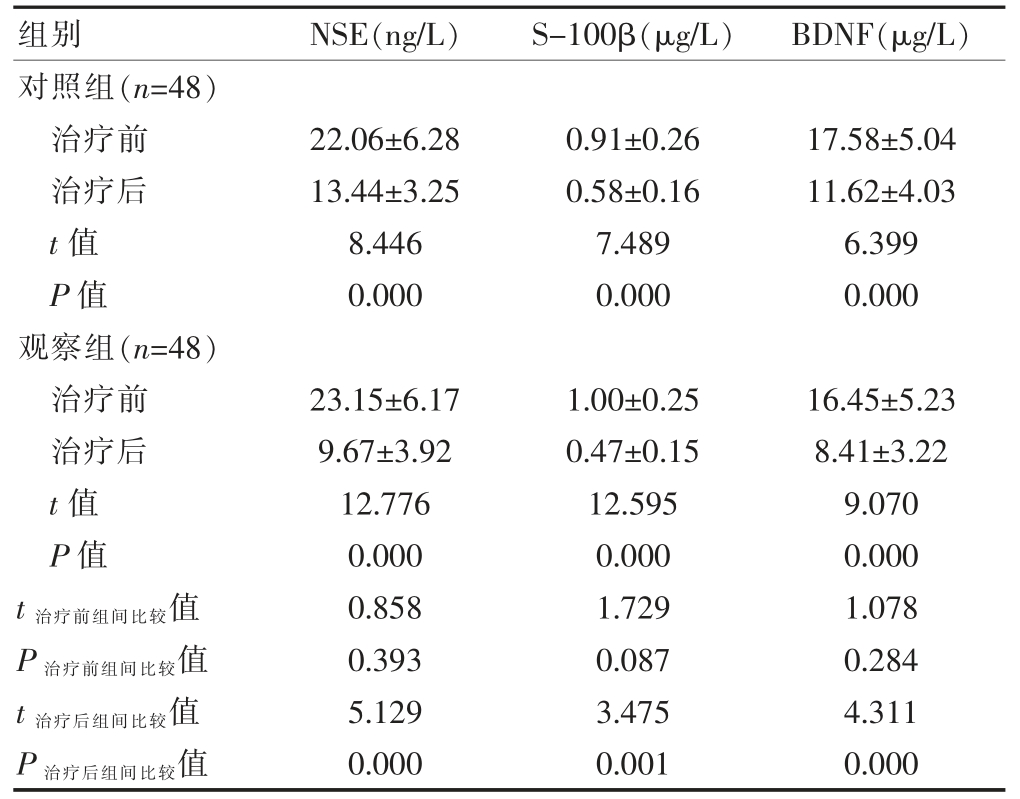
2.4 两组患儿不良反应发生率的比较
观察组发生2 例(4.17%)食欲减退,对照组发生1 例(2.08%)嗜睡,两组患儿的不良反应发生率比较,差异无统计学意义(χ2=0.000,P=0.558)。
3 讨论
惊厥俗称抽风、抽筋、抽搐、惊风等,主要表现为阵发性面部肌肉及四肢抽动,常伴有斜视、凝视或眼球上翻,病情较严重时可能出现面色青紫、呼吸暂停、口吐白沫等症状及体征,发作时间可持续3~5 min。热性惊厥的长期高频发作对患儿智力发育具有较大影响,可能会留下严重后遗症,甚至危及生命[8]。因此,更加安全有效的治疗对患儿及其家庭均具有重要意义。
NSE 为存在于神经组织中的烯醇化酶之一,在神经内分泌及糖酵解过程中起到重要作用。NSE 在脑组织细胞中的活性最高在非神经组织及脊髓液中活性最低。NSE 是一种应用价值较高的分子学标志物,除预示儿童神经母细胞瘤及肺癌外,NSE 活性改变还能够反映同神经损伤而引发的各种神经性疾病,且NSE诊断灵敏性及特异性高达80%~90%,因此,对NSE水平进行监测能够较准确掌握热性惊厥患儿病情发展,是评价疗效、指导治疗的重要指标。S-100 蛋白为酸性钙结合蛋白之一,主要存在于雪旺细胞及神经胶质细胞的细胞液内,因该蛋白可100%溶解饱和硫酸铵,故被称为S-100 蛋白。临床医学研究表明,当神经系统细胞受到损伤后,S-100β 会从细胞液渗入脑脊液中,最终进入血液。因此,S-100β 能够作为中枢神经系统损伤的灵敏生化标志[9]。BDNF 是一种小分子二聚体蛋白质,主要分布于中枢神经系统,周围神经系统、骨组织及内分泌系统中,BDNF 水平升高会导致大脑神经元毒性损伤,因此,通过检测DNF 水平能够判断神经系统健康程度,为临床治疗提供重要指导依据。本研究结果显示,观察组的治疗总有效率(95.83%)高于对照组(83.33%),退热时间早于对照组,差异有统计学意义(P<0.05);治疗后,观察组的NSE、S-100β、BDNF 水平均低于对照组,差异有统计学意义(P<0.05);两组的发热次数及不良反应发生率比较,差异无统计学意义(P>0.05)。提示在常规治疗基础上联合左乙拉西坦治疗小儿热性惊厥,能够显著提升临床疗效,更快缓解患儿发热症状,大幅改善脑神经相关因子水平,且增加用药种类同时保障了安全性,对患儿预后具有积极作用。左乙拉西坦是一种临床应用广泛的成人抗癫痫药,在婴幼儿群体中临床应用相对较少[10-11]。左乙拉西坦通过抑制海马癫痫样突然放电而起效,但不影响正常状态的神经元兴奋,研究发现,本品不会改变T-型钙电流及钠离子通道[12-13]。此外,左乙拉西坦能够对红藻氨酸或毛果芸香碱诱导的局灶性发作继发的全身性发作起到有效保护作用。口服后,左乙拉西坦机体吸收迅速,绝对生物利用率高达100%,且进食时间与进食量对药效不产生影响,因此能够较好适用于婴幼儿群体[14-15]。
综上所述,联合左乙拉西坦治疗小儿热性惊厥,能够显著提升临床疗效,更快缓解患儿发热症状,大幅改善脑神经相关因子水平,安全性较高,对患儿预后具有积极作用。
[参考文献]
[1]王翠玲.热性惊厥的研究进展及合理用药[J].中国临床医生杂志,2017,45(3):18-21.
[2]施莉,黄盛,李玲,等.791 例小儿癫痫的临床特征及缓解率分析[J].癫痫与神经电生理学杂志,2018,27(5):296-301.
[3]吴琼,陈凤仪,杨翠.小儿咽扁颗粒治疗上呼吸道感染伴热性惊厥的临床效果[J].中国医药导报,2019,16(11):73-76.
[4]董玲,李维彬.体质辨识及其在小儿复杂性热性惊厥的临床运用[J].中国中医急症,2019,28(5):917-919.
[5]王和生.左乙拉西坦治疗小儿热性惊厥临床疗效及对患儿脑神经相关因子和免疫功能的影响[J].空军医学杂志,2018,34(3):170-173.
[6]中华医学会儿科学分会神经学组.热性惊厥诊断治疗与管理专家共识2016[J].中华儿科杂志,2016,54(10):723-727.
[7]中华医学会儿科学分会神经学组.热性惊厥诊断治疗与管理专家共识2017 实用版[J].中华实用儿科临床杂志,2017,32(18):1379-1382.
[8]郭伟中.小儿热性惊厥复发的相关因素分析[J].医学综述,2016,22(15):3070-3072.
[9]陈强,陈向坚,叶圣.血清S100B 蛋白与血清NSE 联合检测在小儿热性惊厥中的应用[J].中外医学研究,2016,14(24):48-50.
[10]吴名展,陈伊洁,何素丽,等.左乙拉西坦治疗儿童及青少年癫痫临床分析[J].中国基层医药,2019,26(3):310-314.
[11]杜雅坤,陈芳,王磊,等.左乙拉西坦对部分性癫痫患儿脑电图和认知功能的影响研究[J].中国全科医学,2019,22(14):1689-1695.
[12]孟慧琴.小儿热性惊厥用左乙拉西坦治疗后的复发情况及血清学指标变化研究[J].海南医学院学报,2016,22(9):906-909.
[13]徐晓楠,代珊珊,张妮,等.左乙拉西坦预防小儿热性惊厥复发疗效的Meta 分析[J].临床荟萃,2016,31(7):774-778.
[14]林泽鸿,蔡晓莹,林广裕.地西泮与左乙拉西坦间歇短程治疗预防热性惊厥发作的研究进展[J].中国小儿急救医学,2018,25(1):56-60.
[15]赵海丰,吴艳,吕冰聪,等.左乙拉西坦预防小儿热性惊厥复发的临床效果及安全性研究[J].临床药物治疗杂志,2018,16(2):73-76,92.
Clinical effect of Levetiracetam in the treatment of children with febrile convulsion
LIAO Yue-juan
Department of Pediatrics, Guangdong Provincial People′s Hospital, Zhuhai Hospital, Guangzhou 519000, China
Department of Pediatrics, Guangdong Provincial People′s Hospital, Zhuhai Hospital, Guangzhou 519000, China
[Abstract] Objective To study the clinical effect of Levetiracetam in the treatment of children with febrile convulsion.Methods Ninety-six children with febrile convulsion admitted to our hospital from May 2017 to January 2019 were selected as research objects, and they were divided into control group and observation group according to the random number table method, with 48 cases in each group. The control group was treated routinely, and the observation group was treated with Levetiracetam on the basis of the control group. The clinical efficacy and incidence of adverse reactions in the two groups were compared and analyzed. The symptom relief and levels of brain nerve related factors (neuron-specific enolase [NSE], S-100β protein [S-100β], and brain-derived neurotrophic factor [BDNF]) before and after treatment of the two groups of children were recorded. Results The total effective rate of treatment in the observation group (95.83%) was higher than that in the control group (83.33%), and the antipyretic time was earlier than that in the control group, with statistically significant differences. After treatment, the levels of NSE, S-100β and BDNF in the observation group were lower than those in the control group, and the differences were statistically significant (P<0.05).There were no significant differences in the number of fevers and the incidence rate of adverse reactions in the two groups of children (P>0.05). Conclusion Levetiracetam in the treatment of children with febrile convulsion can significantly improve the clinical efficacy, relieve the symptoms of fever in children, greatly improve the level of brain nerve related factors, and ensure the safety of medication, and have a positive effect on the prognosis of children.
[Key words] Children with febrile convulsion; Levetiracetam; Brain nerve related factors; Epilepsy
[中图分类号]R720.5
[文献标识码]A
[文章编号]1674-4721(2020)2(c)-0103-04
(收稿日期:2019-09-12 本文编辑:任秀兰)