吉非替尼治疗非小细胞肺癌患者的临床效果
黄 超 金 颚 田 宏
沈阳市第四人民医院肿瘤科,辽宁沈阳 110031
[摘要]目的 探讨吉非替尼治疗非小细胞肺癌患者的临床效果。方法 选择2015年3月~2016年5月本院收治的80例非小细胞肺癌患者,按照随机数字表法分为对照组和观察组,各40例。对照组使用GP方案,即吉西他滨联合顺铂方案;观察组使用吉非替尼,比较两组的EGFR突变情况、治疗后角质蛋白19(CYFRA 21-1)及癌胚抗原(CEA)水平变化情况、中位生存时间、生活质量及治疗效果。结果 观察组的突变率显著低于对照组(P<0.05)。观察组治疗后的CYFRA 21-1水平低于对照组(P<0.05),CEA水平低于对照组(P<0.05)。观察组的中位生存时间长于对照组(P<0.05)。观察组的1年及2年生存率均高于对照组,疾病治疗有效率显著高于对照组(P<0.05)。结论针对CEA及CYFRA 21-1水平显著升高的非小细胞肺癌患者,行吉非替尼治疗能有效降低EGFR突变率及肿瘤标志物水平,延长患者生存时间,提高临床治疗效果。
[关键词]吉非替尼;癌胚抗原;角质蛋白19;非小细胞肺癌;EGFR突变率;生存情况
肺癌是目前世界范围内发病率及致死率最高的恶性肿瘤,尤其在我国,随着环境污染加重,雾霾给人们呼吸道带来的影响不容小觑[1]。具相关预测,本病在未来几十年内其发病率还将进一步升高。根据病理学分类,肺癌可分为小细胞肺癌与非小细胞肺癌,其中后者约占80%以上[2],且超过2/3的非小细胞肺癌患者确诊时已处于中晚期,甚至失去手术治疗机会,故本病的5年生存率极低[3]。如何有效提高本病的早期诊断效率,并对患者治疗效果进行预测,是目前的研究重点[4]。随着分子生物学技术的发展,尤其是肿瘤分子生物学及其基因水平的探测,分子靶向治疗药物的临床应用已经成为当今肺癌治疗领域的热点[5]。目前,最常用的分子靶向治疗药物是作用于表皮生长因子受体(EGFR)的靶向治疗药物[6],同时癌胚抗原(CEA)及角质蛋白19(CYFRA 21-1)是目前针对肺癌最常使用的早期诊断指标[7]。为更好地提高非小细胞肺癌患者的诊断效率,指导临床治疗,本研究主要探讨非小细胞肺癌患者治疗前血清CEA和CYFRA 21-1水平与EGFR突变及表皮生长因子受体酪氨酸激酶抑制剂(EGFR-TKI)疗效的关系,现报道如下。
1 资料与方法
1.1 一般资料
选择2015年3月~2016年5月本院收治的80例非小细胞肺癌患者,所有入组者均经纤维支气管镜下镜检并留取活组织病理标本送检后确诊,入组时KPS评分均≥60 分,CEA>5 μg/L,CYFRA 21-1>3.3 μg/L,排除合并全身免疫系统疾病者、治疗前3个月行糖皮质激素治疗者、治疗前3个月行免疫抑制剂治疗者、合并严重肝肾功能障碍者、心力衰竭或心功能不全者、对所用药物过敏者以及签字拒绝入组者。按照随机数字表法将入选患者分为观察组和对照组,各40例。观察组中,男 33例,女7例;年龄 40~75岁,平均(61.3±1.0)岁;病程 3 个月~2 年,平均(5.1±0.2)月;病理类型:腺癌者32例,鳞癌者8例。对照组中,男32例,女8例;年龄 40~75 岁,平均(61.5±1.1)岁;病程 3 个月~2年,平均(5.2±0.2)月;病理类型:腺癌者 33 例,鳞癌者7例。两组的性别、年龄、病程等一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经医院医学伦理委员会批准同意,所有入组患者均知情同意并签署知情同意书。
1.2 治疗方法
所有入组者均行规律化疗,并针对治疗期间出现的不良反应行对症支持处理,化疗方面,对照组使用GP方案即吉西他滨(江苏豪森药业股份有限公司,国药准字 H20030105)联合顺铂(齐鲁制药有限公司,国药准字 H20045501)方案,其中吉西他滨1000 mg/m2静脉滴注30 min,每周1次,连续3周,随后休息1周,每4周重复1次;顺铂每次20 mg/m2,溶于生理盐水20~30 ml中静脉注射,于治疗第1、8天使用,每4周重复1次。观察组使用吉非替尼(阿斯利康制药有限公司,国药准字 J20100014)250 mg(1 片),1 日 1 次,连续治疗4周为1个疗程。当患者病情进展或机体无法耐受继续化疗时停药。
1.3 检验方法
1.3.1 试剂与仪器 DNA提取使用德国Qiagen公司生产的石蜡DNA提取试剂盒,其中人EGFR基因突变的测定使用AmoyDx公司试剂盒进行,CEA与CYFRA21-1检测使用电化学发光法进行,试剂盒由瑞士Roche公司提供。PCR检测仪由美国Bio-Rad公司提供,型号为T100 Thermal Cycler型,电化学发光仪则由瑞士Roche公司提供,型号为E170型。
1.3.2 实验方法 DNA的提取:先行石蜡包埋,并将其制备成5~10 μm厚切片5~10张,并于活检条件下留取新鲜冰冻活体组织2 g,留取相应胸腔积液及外周静脉血标本备检,随后行石蜡DNA提取试剂盒,对新鲜胸腔积液及静脉血标本使用DNA提取试剂盒进行,在获取DNA标本后行洗脱处理,并于NanoDrop 2000分光光度计下进行检测。PCR-Sanger序列测定:使用巢氏PCR法对拟定标本进行基因扩增处理,EGFR基因主要针对第18、19、20和21外显子进行扩增,其中总反应体系容量为25 μl,先于95℃条件下预变性5 min,随后同样温度变性30 s,57℃退火30 s,72℃延伸60 s,通过35个往复循环后,取初次PCR产物2 μl再进行第二次扩增,并经10 g/L琼脂糖凝胶电泳对所得产物进行结果鉴定及测序,以上所有操作均由具有5年以上工作经验的实验员严格按照说明书进行。
1.3.3 结果评定 CEA及CYFRA 21-1浓度测定:所有入组者均留取其清晨空腹肘静脉血2 ml,离心后放入E170型电化学发光仪进行结果检测,其中CEA水平<5 μg/L 评定为正常,≥5 μg/L 评定为升高;CYFRA21-1水平<3.3 μg/L评定为结果正常,≥3.3 μg/L评定为升高。EGFR-TKI治疗价值的评定:结合EGFR突变情况分析,于治疗后8周进行胸部CT复查,评定实体肿瘤治疗情况。实体肿瘤肿瘤疗效评定包括完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),有效率=(CR+PR+SD)例数/总例数×100%。
1.4 统计学方法
采用SPSS 13.0统计学软件对数据进行分析,计量资料以均数±标准差(x±s)表示,两组间均数的比较采用t检验,组间率的比较采用χ2检验,生存时间以中位生存时间表示,采用Kaplan-Meier法、Log rank检验,以P<0.05为差异有统计学意义。
2 结果
2.1 两组EGFR突变情况的比较
观察组的突变例数为21例(52.5%),对照组的突变例数为32例(80.0%)。观察组的突变率显著低于对照组(χ2=6.765,P=0.009<0.05)。
2.2 两组治疗后CYFRA 21-1及CEA水平变化情况的比较
观察组治疗后的CYFRA 21-1水平低于对照组(P<0.05),CEA 水平低于对照组(P<0.05)(表 1)。
表1 两组治疗后CYFRA 21-1及CEA水平变化情况的比较(ng/ml,.jpg) ±s)
±s)

2.3 两组中位生存时间及生活质量的比较
观察组的中位生存时间为(15.6±0.3)个月,对照组的中位生存时间为(8.1±0.4)个月,观察组的中位生存时间长于对照组(t=94.868,P=0.000<0.05)。
2.4 两组2年生存情况的分析
观察组1年存活37例,生存率为92.5%;2年存活25例,生存率为62.5%。对照组1年存活32例,生存率为80.0%;2年存活17例,生存率为42.5%。观察组的1年及2年生存率均高于对照组(P<0.05)(图1,见封四)。
2.5 两组治疗效果的比较
观察组的疾病治疗有效率为82.5%,对照组的疾病治疗有效率为62.5%。观察组的疾病治疗有效率显著高于对照组(χ2=8.717,P=0.003)(表 2)。
表2 两组治疗效果的比较(n)
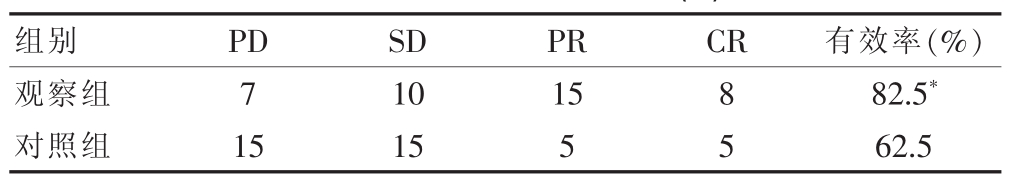
与对照组比较,*P<0.05
3 讨论
近年来针对进展期非小细胞肺癌以及治疗后复发的非小细胞肺癌者,使用EGFR-TKI具有较好的临床效果[8];而对于末经选择晚期非小细胞肺癌患者,使用EGFR-TKI则其有效率较低[9]。研究提示EGFR-TKI主要通过与三磷酸腺苷竞争胞内酪氨酸激酶活性位点从而抑制胞内酪氨酸激酶磷酸化过程[10],与阻断机体EGFR信号转导,抑制肿瘤细胞的增殖以及肿瘤组织血管的生成有关[11]。目前临床常用的EGFR-TKI为吉非替尼,故本研究观察组联合应用吉非替尼[12]。
以往研究显示[13],非小细胞肺癌患者过度表达的EGFR,将导致其对化疗与放疗均不敏感,进而导致早期的远处转移等。在EGFR-TKI选择方面,本研究观察组使用吉非替尼,并通过治疗前后测定EGFR突变情况,结合患者生存时间、临床治疗效果等进行综合分析,结果显示,观察组的EGFR突变率显著低于对照组,且治疗后,观察组的CYFRA 21-1水平低于对照组,CEA水平低于对照组,提示针对非小细胞肺癌患者行吉非替尼治疗后能有效降低EGFR突变率及机体肿瘤相关标志物水平。另外,针对生存时间的研究发现,观察组的中位生存时间长于对照组,且观察组1年及2年生存率均高于对照组,观察组的疾病治疗有效率显著高于对照组,提示针对非小细胞肺癌患者行吉非替尼治疗,可显著延长患者生存时间,提高整体疗效。本研究中,观察组使用的吉非替尼为EGFR络氨酸激酶可逆性拮抗剂,是首个应用于非小细胞肺癌治疗的EGFR酪氨酸激酶抑制剂,被临床广泛认识[14]。可能与使用的吉非替尼能够有效透过多种机体屏障,如血-脑脊液屏障等,故可以提高临床治疗效果[15]。另外,使用吉非替尼后,其能有效竞争催化区域上Mg-ATP结合位点,阻断其信号传递,且抑制有丝分裂原活化蛋白激酶的活化,促进细胞凋亡等,故观察组生存时间延长、临床治疗效果提高。小分子酪氨酸激酶抑制剂靶向分子的表达水平以及其突变情况对于吉非替尼治疗的临床效果影响极大,观察组使用吉非替尼后能够广泛抑制肿瘤细胞转移与种植,同时抑制其增殖,且提高化放疗与激素治疗效果。
综上所述,针对CEA及CYFRA 21-1水平显著升高的非小细胞肺癌患者,行吉非替尼治疗能有效降低EGFR突变率及肿瘤标志物水平,延长患者生存时间,提高临床治疗效果。
[参考文献]
[1]王群慧,郑华,胡范彬,等.伴有EGFR突变的非小细胞肺癌血清CYFRA21-1和CEA水平与EGFR-TKIs的疗效关系[J].中国肺癌杂志,2016,19(8):550-558.
[2]韩涛,杨晓丹,谢晓冬,等.DC-CIK细胞联合EGFR TKI治疗EGFR突变阳性进展期非小细胞肺癌的疗效[J].中国肿瘤生物治疗杂志,2016,23(3):408-412.
[3]Zhou G,Zhang F,Guo Y,et al.miR-200c enhances sensitivity of drug-resistant non-small cell lung cancer to gefitinib by suppression of PI3K/Akt signaling pathway and inhibites cell migration via targeting ZEB1[J].Biomed Pharmacother,2016,5(85):113-119.
[4]Pakkala S,Ramalingam SS.Epidermal growth factor receptor mutated advanced non-small cell lung cancer:a changing treatment paradigm[J].Hematol Oncol Clin North Am,2017,31(1):83-99.
[5]林景辉,何志勇,林动,等.EGFR-TKI治疗EGFR突变的Ⅳ期NSCLC的临床观察[J].齐齐哈尔医学院学报,2016,37(15):1881-1885.
[6]赵钊,陈盼盼,张萍.NSCLC患者EGFR基因突变与血清肿瘤标志物相关性分析研究[J].中国卫生检验杂志,2014,24(15):2217-2222.
[7]王娜,郑清,孙成铭,等.非小细胞肺癌EGFR基因突变的表现及其与肿瘤标记物的相关性[J].现代肿瘤医学,2016,24(19):3053-3056.
[8]林顺欢,江冠铭,刘淳,等.贝伐珠单抗联合EGFR-TKI治疗EGFR外显子19或21突变晚期非小细胞肺癌的疗效差异[J].新医学,2016,47(7):472-476.
[9]黄宇筠,袁润强,陈应智,等.非小细胞肺癌基因突变与扩增的比较及其与血清水平的关系[J].分子诊断与治疗杂志,2015,7(1):22-26.
[10]肖何,王阁,王东,等.非小细胞肺癌血浆 EGFR突变与肿瘤标志物水平的关系[J].第三军医大学学报,2013,35(14):1520-1523.
[11]刘宁,张康,颜淑霞,等.非小细胞肺癌EGFR基因突变及与疗效的相关性研究[J].现代肿瘤医学,2013,21(2):330-333.
[12]李焕焕,马晓平,林芷伊,等.首次复发NSCLC患者血清CEA水平与EGF-TKI疗效相关性分析[J].中华肿瘤防治杂志,2015,22(4):281-284.
[13]张连民,郝李刚,张华,等.血清癌胚抗原与非小细胞肺癌患者EGFR突变的关系及其对预后的影响[J].中国肿瘤临床,2014,41(17):1075-1079.
[14]钟文昭,李巍,董嵩,等.血清CEA水平在EGFR-TKI治疗非小细胞肺癌的应用价值[J].临床与病理杂志,2015,35(6):951-959.
[15]Huang A,Li R,Zhao J,et al.Epidermal growth factor receptor (EGFR)-tyrosine kinase inhibitors combined with chemotherapy in first-line treatment in an advanced nonsmall cell lung cancer patient with EGFR sensitive mutation[J].Thorac Cancer,2016,7(5):614-618.
Clinical effect of Gefitinib in the treatment of patients with non-small cell lung cancer
HUANG ChaoJIN E TIAN Hong
Department of Oncology,the Fourth People′s Hospital of Shenyang City in Liaoning Province,Shenyang 110031,China
Department of Oncology,the Fourth People′s Hospital of Shenyang City in Liaoning Province,Shenyang 110031,China
[Abstract]Objective To investigate the clinical effect of Gefitinib in the treatment of patients with non-small cell lung cancer(NSCLC).Methods A total of 80 patients with NSCLC admitted to our hospital from March 2015 to May 2016 were enrolled in this study.They were divided into the control group and the the observation group according to a random number table method,40 cases in each group.The control group was treated with GP regimen,Gemcitabine combined with Cisplatin regimen,while the observation group was treated with Gefitinib.The epidermal growth factor receptor(EGFR)mutations in the two groups were compared.The keratin 19(CYFRA 21-1)and carcinoembryonic antigen(CEA)levels after treatment,and median survival time,quality of life,and therapeutic effect of the two groups were compared.Results The mutation rate of the observation group was significantly lower than that of the control group(P<0.05).The levels of CYFRA 21-1 and CEA in the observation group were lower than those of the control group (P<0.05).The survival time of the observation group was longer than that of the control group(P<0.05).The 1-year and 2-year survival rates of the observation group were both higher than those of the control group(P<0.05).The effectiveness rate of disease treatment in the observation group was significantly higher compared with that of the control group (P<0.05).Conclusion In NSCLC patients with markedly elevated CEA and CYFRA 21-1 levels,Gefitinib treatment can effectively reduce EGFR mutation rate,reduce tumor marker levels,prolong patient′s survival time,and improve the clinical therapeutic effect.
[Key words]Gefitinib;Carcinoembryonic antigen;Keratin 19;Non-small cell lung cancer;Epeidermal growth factor receptor mutation rate;Survival
[中图分类号]R734.2
[文献标识码]A
[文章编号]1674-4721(2019)1(b)-0064-04
(收稿日期:2018-07-09本文编辑:祁海文)